青光眼是全球首位不可逆性致盲眼病,其临床特征是视神经头病变和视野丧失。与其它神经退行性疾病相似,青光眼的发病机制复杂多样。有文献表明,在青光眼患者视网膜中编码缝隙连接蛋白43(connix43,Cx43)的缝隙连接α1基因存在突变,但是,Cx43如何参与青光眼视网膜神经节细胞的损伤仍然未知。
近日,复旦大学脑科学研究院王中峰课题组在国际期刊《胶质细胞》(Glia)上在线发表了题为《调控Rac1/PAK1/connexin43介导的星形胶质ATP释放参与实验性青光眼神经节细胞的存活》(Modulation of Rac1/PAK1/connexin43-mediated ATP release from astrocytes contributes to retinal ganglion cell survival in experimental glaucoma)的研究论文。
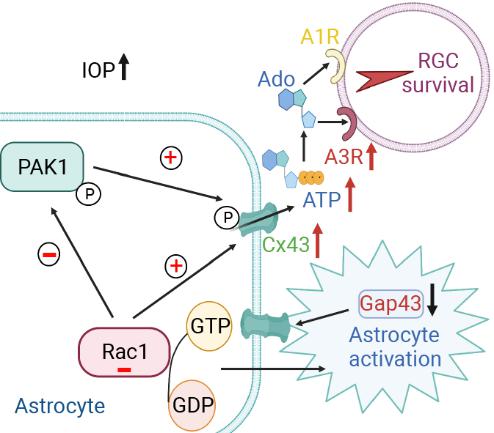
Cx43是胶质细胞中的一种主要缝隙连接蛋白,通过组成缝隙链接或半通道,介导小分子物质、胶质递质等在细胞间的转移,参与维持细胞和组织的稳态。他们的研究工作发现,Cx43主要表达在视网膜星形胶质细胞上。在慢性高眼压实验性青光眼小鼠模型中,视网膜Cx43表达下调,与视神经中星形胶质细胞的可塑性下调有关。小G蛋白Rac1或下游靶分子PAK1负性调节Cx43表达、Cx43半通道开放和星形胶质细胞激活。药理学抑制Rac1或条件性敲除星形胶质细胞的Rac1可增加Cx43半通道开放和ATP释放,进而激活视网膜神经节细胞的腺苷A3受体,促进视网膜神经节细胞的存活。这些结果提示,星形胶质细胞通过Rac1/PAK1/Cx43/ATP信号通路参与视网膜神经节细胞的损伤。研究成果为青光眼的临床治疗提供了新的思路。
脑科学研究院博士研究生赵国丽为论文第一作者,苗艳颖副研究员和王中峰研究员为论文共同通讯作者。本工作得到国家自然科学基金委、上海市科技重大项目、张江实验室及深圳“三名”工程等的资助。